什么是大π键?如何理解它?
xiang详细解释:多个π轨道或π轨道与p轨道平行重叠形成大π键,例如1,3-丁二烯,1,2碳之间的π轨道,和3,4碳之间的π轨道平行重叠形成(或4个碳的p轨道),苯中6个碳的2p轨道平行重叠形成环状π键,再如硝酸根中,氮(2s。
苯的大π键具体是怎么回事?
苯的大π键具体是怎么回事? 请回答的详细一些,本人喜欢化学,但是又很。苯的大π键的形成使π键电子云为6个碳原子所共有,因而受到6个碳原子核的共同吸引,彼此结合得比较牢固。
同时,苯的大π键是平均分布在6个碳原子上,所以苯分子中每个碳碳键的键长和键能是相等的。
π键类型 1、离域π。
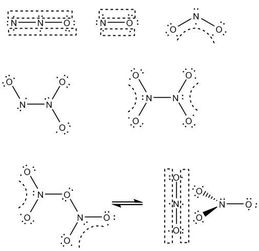
什么是大∏键
苯的大π键是平均分布在六个碳原子上 所以苯分子中每个碳碳键的键长和键能是相等的 又如,丁二烯分子式为H2C=CH-CH=CH2.4个碳原子均与3 个原子相邻 故采用sp2杂化 这些杂化轨道相互重叠 形成分子σ骨架 故所有原子处于。
化学,大派键是什么?派键是什么?
1、大派键:在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离域π键,或共轭大π键,简称大π键。
2、派键:原子轨道。
分子结构中大π键是如何形成的?有什么作用?
是因为硝酸根还有一个负电荷。
环戊二烯负离子中的大π键是两个π键(4个p轨道,每个p轨道含有一个电子),和一个含油量和电子的p轨道(碳负离子)平行重叠形成的。
烯丙基碳正离子,环庚三烯正离子,臭氧等均具有大π。
